衛生福利部、國家衛生研究院、及羅氏大藥廠攜手打造台灣精準醫療生態系 (原始連結)
公告重點擷錄
癌症一直高居國人十大死因首位,而醫學上在癌症治療之進步也與日俱進,尤其臺灣醫療環境優良,又有健保制度,癌症治療品質也持續進步。現在的癌症治療已經邁入精準醫療階段,讓藥品能夠更發揮療效而減少浪費,進入個人化醫療則是許多先進國家在醫療上之終極目標。
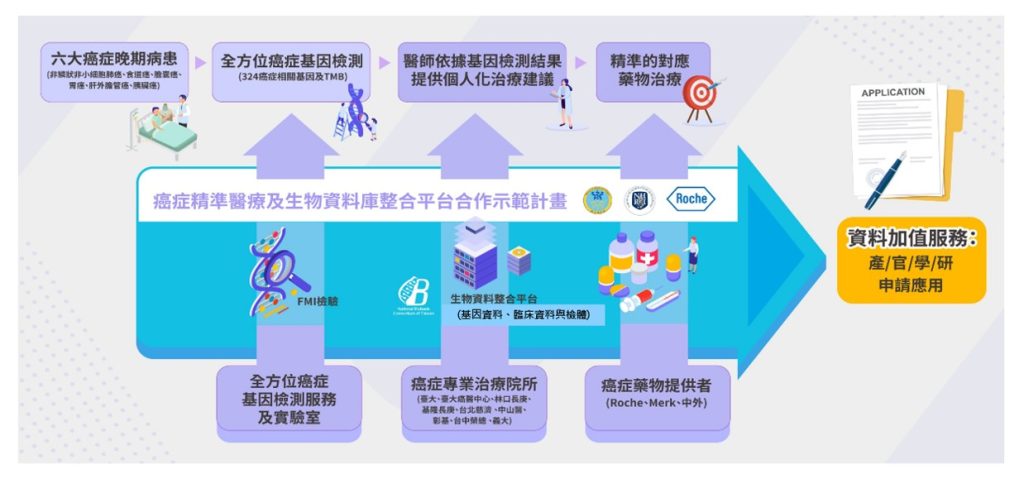
本「癌症精準醫療及生物資料庫整合平台合作示範計畫」(以下簡稱示範計畫)是由羅氏大藥廠與國家級人體生物資料庫整合平台(以下簡稱整合平台 = NBCT)合作建立個人化精準醫療模型範本,並建立精準醫療用藥評估機制,因此先針對特定癌別之治療。透過次世代基因定序(NGS)檢測,讓醫師可以根據基因檢測報告資訊與癌症精準醫療臨床小組之建議,進行臨床醫療決策,使病人獲得最合適之治療選擇。
此示範計畫將同時收集這些病患的基因數據及臨床醫療結果資料(真實世界數據real world data),儲存在各收案醫院之人體生物資料庫,再透過整合平台建立的醫療大數據共同資料欄位模式,未來可以由整合平台彙整各醫院之數據,建立可永續發展之國家級基因醫療大數據庫(下稱大數據庫)。
透過整合平台建立此精準醫療大數據庫將有助於強化台灣之醫療品質,提供臨床醫師更多決策依據之參考;未來也能以產業友善之方式申請應用,以加速產業升級。另透過本計畫,未來推動運用真實世界證據作為藥物研發、藥品上市登記及健保給付評估之機制。
醫院參與本計畫之條件
1.參與醫院認同本計畫精神
2.必須是參與國家級人體生物資料庫整合平台 (NBCT) 之醫療機構
3.參與醫院之本計畫收案癌症病人數目充足
4.參與醫院需成立癌症精準醫療臨床小組 (MTB)
5.參與醫院願意配合建立整合平台為其人體生物資料庫所設計之醫療大數據共同模式 (CDM)
6.參與醫院之人體生物資料庫需能夠配合收集本計劃要求之醫療數據 (包含New Variable),並確保資料正確性與 完整性。醫療數據內容參見附件。
7.參與醫院之人體生物資料庫同意接受整合平台轉介之羅氏大藥廠醫療數據研究申請案,依整合平台之標準申請流程出庫。
本計畫由國家級人體生物資料庫整合平台負責,串連全台灣北中南12家醫院 :其中臺大醫院 (含臺大癌醫中心分院)、林口長庚醫院、基隆長庚醫院、台北慈濟醫院、台中榮民總醫院、中山醫學大學附設醫院、彰化基督教醫院、義大醫院、打造個人化精準醫療網,並已開始收案執行。 [高雄榮民總醫院,高雄長庚醫院,高雄醫學大學附設醫院、台北醫學大學附設醫院體系也即將開始加入收案行列。] (as of 2022/08/05)
計畫收案標準與人數
| 癌別 | 期別 | 人數+ |
|---|---|---|
| 非鱗狀非小細胞肺癌(排除EGFR陽性、排除ALK陽性及排除ROS1陽性之病人) | IIIB以上 | 1,000 |
| 食道癌 | IIIB以上 | 250 |
| 膽囊癌 | IIIB以上 | 225 |
| 胃癌 | IIIB以上 | 150 |
| 肝外膽管癌 | IIIB以上 | 225 |
| 胰臟癌 | III以上 | 150 |
- 本計畫將由羅氏大藥廠提供整合平台2,000例之FMI基因檢測(FoundationOne® CDx)給予本計畫之收案對象;各醫院收案病人數量無限制,唯總收案病人數不超過2,000例。
- 本計畫預計執行期間,以全台灣第一名收案病人接受Foundation medicine, Inc.( FMI ) 的全方位癌症基因檢測套組(FoundationOne® CDx)起算 (110年10月),至最後一名收案病人接受FMI檢測後追蹤滿十二個月為止。
- 本計畫收案期間,以收案病人數達2,000人或是計畫開始執行期滿兩年其中之一先達成者為止。
- 初診斷及首次復發後尚未接受系統性治療*(化學治療、標靶治療)之下列癌症病人 (年滿20歲以上)
- 在診斷為IIIB以上(晚期)收案時,不能有用過systemic treatment 即可,病人在疾病早期使用過neo-adjuvant, adjuvant or CCRT 不在排除條件。
- 可納入接受過手術、輔助性化療或局部放射線治療之病人,但是必須與輔助性化療或局部放射線治療經歷無療程間隔至少 12 個月。
- +第一年收案以1,000例為上限(肺癌500例、食道癌125例、膽囊癌110例、胃癌75例、肝外膽管癌115例、胰臟癌75例),第二年上述各癌別數量比例則不在此限。

- FMI基因檢測(FoundationOne® CDx)採集檢體的方式,檢體內容和檢體數量及頻率:此基因檢測須向病理科申請病人的腫瘤檢體之「石蠟空白切片」大約「10-15片」,本計畫對一個病例只提供一次基因檢測。
- 這是本計畫的一大門檻,檢體可以來自原發腫瘤 或是 轉移部位的腫瘤, 但是不能混在一起送檢測
- 本計畫採集之腫瘤切片檢體僅供FMI基因檢測(FoundationOne® CDx)使用,不會收集非腫瘤檢體,也不會保存腫瘤檢體。
研究預期效益(對病人的告知)
本研究計畫提供之(FMI)的全方位癌症基因檢測套組(FoundationOne® CDx)】可以檢測324 個和癌症相關的基因變化 (包含基因變異,TMB,CNV),以期能找出可以當作用藥參考的基因突變。此檢測套組已在美國食藥署審查通過,認定其報告內容可以當作醫師診療用藥的參考依據。所以此項基因檢測結果對於您的治療決策將有幫助,可以幫助醫師選擇最適合的治療方式。請了解此項檢測也可能找不到任何可以用藥的突變。此研究所建立之精準醫療大數據庫將提供臨床醫師更多決策依據之參考,有助於強化台灣之醫療品質,所以將來也對於跟您患同樣疾病患者之治療有益處。另透過本計畫建立的醫療大數據,對於未來推動運用真實世界證據作為藥物研發、藥品上市登記及健保給付評估都會有助益。
贈藥

羅氏藥廠,台灣默克集團、台灣中外製藥,台灣禮來亦共同加入示範計畫,將依基因檢測結果,提供他們最適合的癌症標靶用藥給參與此計畫的病患。
透過跨癌別的全方位基因檢測、智慧化分析,讓醫師據以進行精準臨床醫療決策,使病人獲得最合適之治療選擇,再搭配後端精準醫療用藥的合作,對癌症病人有非常大的助益,也是精準醫療的完美呈現。
這兩千例全方位基因檢測的投入,對於全台標靶治療藥物的臨床試驗收案及個人化精準醫療的推展極有助益,是一個讓病人,醫師和藥廠三贏的最佳策略。
目前正持續邀請 其他有相關標靶藥物的國際大藥廠 參與贈藥。
癌症精準醫療臨床小組 (Molecular Tumor Board, MTB)
- MTB職責:
- 即時提供示範計畫病人主治醫師諮詢及診療建議
- 評估病人是否符合示範計畫藥廠贈藥申請資格
- 形式
- MTB設置要點
- 頻率 : 至少一個月一次
- 各家醫院自己設立。
| 成員 | 職責 |
|---|---|
| 主持人(臨床醫師) | 帶領小組討論 |
| 主治醫師 | 報告收案病人診斷與病史 |
| 分子生物學專家 | 報告收案病人變異基因之訊息傳遞路徑與對應藥物資訊 |
| 跨專科臨床醫師 | 提供臨床治療之建議 |

大數據共同資料模式 Common Data Model (CDM)
- 規劃資料欄位,能夠分析病人疾病診斷、治療及預後追蹤的資訊 (to assemble a model of common data elements for EHRs
- 促進資料的互通性 (to facilitate data interoperability for patient care and research)
- 維持足夠的資料品質 (to maintain sufficient data quality)
介紹 (原始連結)
為了配合國家級人體生物資料庫整合平台,收集臨床治療追蹤資料,以提升人體生物資料庫最大利基,研究團隊協助各醫療機構之人體生物資料庫,建置電子健康數據的共同欄位內容。建置過程如圖一所示,先由各機構的資訊同仁擷取將其機構內人體生物資料庫所收錄的病人的醫療資料(醫院電子病歷資料庫及癌症登記資料庫)匯入機構內的人體生物資料庫(如:圖一①),機構內對於資料的收集、處理及使用是依照人體生物資料庫管理條例的規定,整合平台研究團隊提供資料處理系統(程式軟體)給各機構人體生物資料庫進行轉檔,並以整合平台所設定的共同資料模式(common data model, CDM),經去識別後存放於機構內人體生物資料庫不連網路的電腦中(如:圖一②),整合平台研究團隊之資料處理系統(程式軟體)也同時提供功能將共同資料模式彙整成各項主題檔案(如:breast cancer, colorectal cancer, etc)(如:圖一③),提供給通過審查的申請者使用,提供給申請者之前,先將資料彙整於整合平台,經二次加密(個人代碼重新編碼)(如:圖一④),後再提供給申請者(如:圖一⑤)。
癌症共通資料模式的建置,除了是跨醫療機構資料欄位的一致性之外,其「共通」的意義也是包含各種癌症治療過程,並不需要依據不同癌症設計不同的欄位,因此必須在避免太過龐大的資料模組前提下,同時需要包含各種療程的追縱,而不同癌症或不同治療的特定療效分析研究,再由共同資料模組中的資料庫設計完成;研究團隊參考國際上精準醫療研究用於收集癌症診療資訊mCODE (Minimal Common Oncology Data Elements)的資料欄位內容,主要分成:patient、disease、genomics、treatment、lab/vital and outcome等六個部分(圖二),規劃格式一致化的共同資料欄位(common data model)。
上述欄位項目中,醫療機構有的癌症登記資料,登錄了在診斷、分期及處置部分,醫療機構已經有癌症登記檔可以提供建構;在medications ordered、medications administered、radiation therapy 及手術部分的欄位,是屬於醫療處置的資料也是醫療機構固定上傳健保署的申報資料,每個病人的資料筆數會隨著時間持續累積,然而若不是在健保給付的範圍內,則不在上傳的資料中;在laboratory tests及vital signs部分,各醫療機構都會有這些資料,同時每個病人的資料也都是需要持續累積;而imaging/radiology reports部分,在醫療機構會幾乎都是文字報告的非結構式 (unstructured) 資料,因此如何擷取所需要的資訊,就會是個挑戰;解決的方式可以進行自然語言處理 (natural language processing,NLP),以摘錄(abstraction)出結構式 (structured) 欄位資料。
新興癌症藥品的治療,除了存活率之外,更強調的是腫瘤對治療的反應(tumor response)、無腫瘤狀態的維持(disease-free)、腫瘤無惡化的維持(progression-free)以及藥物副作用(toxicity, adverse events),因此對於癌症病人治療的結果評估,不再只是局限於存活率,病人經過癌症治療後,結果(outcome)是stable、worsening (progressing) 或是improving (responding),在臨床治療上,往往需要多種臨床資料如:影像資料、assessment of symptoms、腫瘤標記(tumor markers)、檢驗檢查資料等,來判定是progression-free survival (PFS)、time to progression (TTP)、time to treatment failure (TTF)、event-free survival (EFS)、time to next treatment (TTNT)、objective response rate (ORR);同時,而治療上引起的toxicity/adverse events (Common Terminology Criteria for Adverse Events,CTCAE) 也是同樣需要結構性與非結構性的資料; 以目前醫療院所的結構性資料內容,足以判定存活率,而PFS及TTF則有賴各癌症中心是否有定期維護癌症病人的個案管理追蹤資料檔料,登錄「復發狀態」及「治療反應」, 此外透過治療及用藥紀錄的分析追蹤,可以取得TTNT,因此完整資料仍有待非結構式資料的整理,因此在第一階段設定醫療數據的共同資料欄位時,是以結構式資料欄位為先(圖二)。
由於各醫療機構數據量龐大且複雜,為將醫療機構資訊同仁整理資料欄位的負擔降至最低,NBCT CDM的資料欄位主要以現有的政府單位規範格式為基礎進行規劃,如例行上傳中央健康保險署的門診、住院、檢驗(查)申報格式,以及上傳國民健康署的癌症登記長短表等為主要的資料來源(圖三)。後續提供給資料申請者的臨床資料,可以整合平台的分散式系統出庫(圖四)。
安裝在醫療機構內的NBCT系統(圖五),主要目的是醫療機構的數據資料不需要離開醫院就可以順利轉檔成NBCT CDM,並依照人體生物資料庫管理準則進行資料處理,NBCT CDM資料處理系統功能摘要說明如下:
- 電子病歷資料整合與檢核: 收整醫院整合完成之電子病歷或CDM格式資料,經由第一階段的資料內容檢核與驗證、去識別化,確保研究資料庫的安全性、完整性與正確性,協助提升資料品質(圖六)。
- 數據庫資料視覺化: 即時分析CDM資料項目,以視覺化呈現說明現有資料量,提供人體生物資料庫同仁進行查詢(圖七)。
- 主題式資料庫萃取: 建構主題式資料庫包含疾病診斷、疾病歷史、檢驗檢查、醫囑、處置、藥囑、用藥、癌症資料等不同面向之條件篩選,提供檢索及臨床研究資料萃取(圖八)。
- CDM出庫與研究應用: 將出庫資料完成整合與整理,並提供加解密流程,以因應資料安全與保護措施。
病歷資料登錄
- 本計畫所需收集的醫療數據中,大部分透過整合平台(NBCT)建立的CDM取得,少部分無法透過CDM取得,需由個管師協助進行病歷抄錄。
- 使用程式:Microsoft Access「示範計畫病歷資料抄錄表單.accdb」(以下簡稱Access表單)
- 於個案每次回診抄錄新資料,需確認每份表單是否有新資料要填寫。
- Access表單收集之資料,後續會儲存至人體生物資料庫*,供後續申請運用。
病歷資料收集清單
- 1 Patient demographic 個案基本資料
- 2-1 Cancer characteristic (newly diagnosis) 癌症基本特性(初診斷個案)
- 2-2 Cancer characteristic (recurrence) 癌症基本特性(復發個案)
- 3 Performance status 體能狀態
- 4. Co-morbidities
- 5. Laboratory results
- 6. Biomarker test
- 7. Cancer related medication
- 7-1 Stopping reason for cancer related medication (inpatient) 癌症相關藥物治療之停藥原因(住院)
- 7-2 Stopping reason for cancer related medication (outpatient) 癌症相關藥物治療停藥原因(門診)
- 8. Co-medication
- 9. Cancer related radiotherapy 癌症相關放射治療
- 10 Cancer related surgery
- 11. Cancer treatment outcome 癌症治療結果
- 12. Follow-ups 癌症追蹤日期
- 13. Death data
- 14. Value indicator of the project 計畫評估指標
- (紅字標示者為自CDM自動擷取之項目,不需人工抄錄)